Hifair® Smearase 高通量测序酶切试剂 片段化酶
产品说明书
FAQ
COA
已发表文献
Hieff ® Smearase 是针对高通量测序平台设计的新一代酶切试剂。本品采用高质量的片段化酶,酶切效果稳定,偏好性 低,可有效降低片段化的时间和成本,摆脱了繁琐的超声步骤,让片段化过程变得更加简单高效。
产品组分
|
组分编号 |
组分名称 |
8 T |
24 T |
96 T |
|
12907 |
Hieff ® Smearase |
80 μL |
240 μL |
960 μL |
运输和保存方法
冰袋运输。
-20℃保存,有效期 1 年。
注意事项
1. 本试剂盒兼容范围为 1 ng – 1 μg Input DNA。应尽可能使用 A260/A280 = 1.8-2.0 的高质量 Input DNA。
2. 若 Input DNA 中引入高浓度金属离子螯合剂或其他盐,可能会影响后续实验,建议将 DNA 稀释在 ddH2O 或不含 EDTA
的 10 mM Tris Buffer (pH 7.5-8.0)中进行片段化,EDTA 耐受范围为 0-2 mM。
3. 对于常规的高质量基因组 DNA,酶切时间参考表 1。本试剂盒片段化偏好低,耐受各种 GC 含量的模板。
表 1 常规基因组 DNA 片段化时间推荐表
|
插入片段主峰大小 |
片段化时间 |
优化范围 |
|
600 bp |
5 min |
3-10 min |
|
400 bp |
10 min |
8-15 min |
|
250 bp |
15 min |
10-20 min |
|
200 bp |
20 min |
12-25 min |
|
150 bp |
25 min |
20-30 min |
【注】:以上为推荐时间,需客户在自己的实验体系中进行微调,以达到最佳效果。
4. 参考表 1 片段化时间可将 DNA 酶切为所需大小,为保证优质稳定的片段化效果,片段化过程请于冰上操作。
5. 该酶在高温条件下即可失活。
6. 为了您的安全和健康,请穿实验服并戴一次性手套操作。
7.本产品仅作科研用途!
使用方法
DNA 片段化(DNA Fragment)
该步骤将基因组 DNA 片段化。
1. 将表 2 中试剂解冻后,颠倒混匀,置于冰上备用。
2. 于冰上配制表 2 反应体系。
表 2 DNA 片段化 PCR 反应体系
|
名称 |
体积(μL) |
|
Input DNA |
x |
|
Hieff ® Smearase |
10 |
|
ddH2O |
Up to 60 μL |
3. 使用移液器轻轻吹打或振荡混匀,并短暂离心将反应液离心至管底。
4. 将上述 PCR 管置于 PCR 仪,设置表 3 所示反应程序,进行 DNA 片段化反应。
表 3 DNA 片段化 PCR 反应程序
|
温度 |
体积(μL) |
|
热盖 105°C |
On |
|
4 °C |
1 min* |
|
30 °C |
3-30 min** |
|
72 °C |
10 min |
|
4 °C |
Hold |
【注】:*DNA 片段化过程为有效控制片段化效果,避免过度酶切,反应程序可预先设置 4℃,待模块温度降至 4℃时,将 PCR 管放入 PCR 仪即可。
**对于完整的基因组 DNA,酶切时间参考表 1。
5. 产物如需纯化,可使用 Hieff NGS® DNA Selection Beads(Cat#12601)或 AMPure XP Beads(Cat#A63880)或其他等效产 品。
参考实例
使用 Hieff ® Smearase 对 Human gDNA 样本进行酶切,片段化结果见图 1。

图 1 Hieff ® Smearase 酶切 200 ng Human gDNA 样本(不同酶切时间片段化效果检测)
HB210527
Hieff ® Smearase 是针对高通量测序平台设计的新一代酶切试剂。本品采用高质量的片段化酶,酶切效果稳定,偏好性 低,可有效降低片段化的时间和成本,摆脱了繁琐的超声步骤,让片段化过程变得更加简单高效。
产品组分
|
组分编号 |
组分名称 |
8 T |
24 T |
96 T |
|
12907 |
Hieff ® Smearase |
80 μL |
240 μL |
960 μL |
运输和保存方法
冰袋运输。
-20℃保存,有效期 1 年。
注意事项
1. 本试剂盒兼容范围为 1 ng – 1 μg Input DNA。应尽可能使用 A260/A280 = 1.8-2.0 的高质量 Input DNA。
2. 若 Input DNA 中引入高浓度金属离子螯合剂或其他盐,可能会影响后续实验,建议将 DNA 稀释在 ddH2O 或不含 EDTA
的 10 mM Tris Buffer (pH 7.5-8.0)中进行片段化,EDTA 耐受范围为 0-2 mM。
3. 对于常规的高质量基因组 DNA,酶切时间参考表 1。本试剂盒片段化偏好低,耐受各种 GC 含量的模板。
表 1 常规基因组 DNA 片段化时间推荐表
|
插入片段主峰大小 |
片段化时间 |
优化范围 |
|
600 bp |
5 min |
3-10 min |
|
400 bp |
10 min |
8-15 min |
|
250 bp |
15 min |
10-20 min |
|
200 bp |
20 min |
12-25 min |
|
150 bp |
25 min |
20-30 min |
【注】:以上为推荐时间,需客户在自己的实验体系中进行微调,以达到最佳效果。
4. 参考表 1 片段化时间可将 DNA 酶切为所需大小,为保证优质稳定的片段化效果,片段化过程请于冰上操作。
5. 该酶在高温条件下即可失活。
6. 为了您的安全和健康,请穿实验服并戴一次性手套操作。
7.本产品仅作科研用途!
使用方法
DNA 片段化(DNA Fragment)
该步骤将基因组 DNA 片段化。
1. 将表 2 中试剂解冻后,颠倒混匀,置于冰上备用。
2. 于冰上配制表 2 反应体系。
表 2 DNA 片段化 PCR 反应体系
|
名称 |
体积(μL) |
|
Input DNA |
x |
|
Hieff ® Smearase |
10 |
|
ddH2O |
Up to 60 μL |
3. 使用移液器轻轻吹打或振荡混匀,并短暂离心将反应液离心至管底。
4. 将上述 PCR 管置于 PCR 仪,设置表 3 所示反应程序,进行 DNA 片段化反应。
表 3 DNA 片段化 PCR 反应程序
|
温度 |
体积(μL) |
|
热盖 105°C |
On |
|
4 °C |
1 min* |
|
30 °C |
3-30 min** |
|
72 °C |
10 min |
|
4 °C |
Hold |
【注】:*DNA 片段化过程为有效控制片段化效果,避免过度酶切,反应程序可预先设置 4℃,待模块温度降至 4℃时,将 PCR 管放入 PCR 仪即可。
**对于完整的基因组 DNA,酶切时间参考表 1。
5. 产物如需纯化,可使用 Hieff NGS® DNA Selection Beads(Cat#12601)或 AMPure XP Beads(Cat#A63880)或其他等效产 品。
参考实例
使用 Hieff ® Smearase 对 Human gDNA 样本进行酶切,片段化结果见图 1。
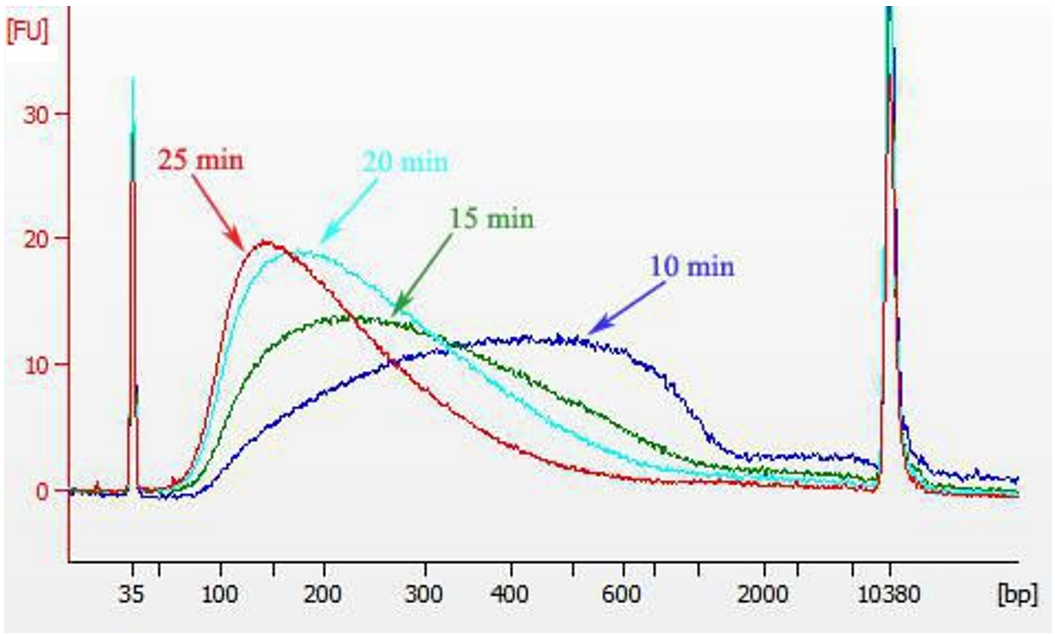
图 1 Hieff ® Smearase 酶切 200 ng Human gDNA 样本(不同酶切时间片段化效果检测)
HB210527
Q:12204ES、12907ES 和 12609ES 区别与联系?
A:12204 为完整的建库试剂盒,包含片段化模块,连接模块,扩增模块。12609 为片段化模块,可同时进行样本的片段化,末端修复/加A流程。12907 为单酶(原料酶),仅用于DNA 片段化。
Q:12907里面的酶是什么酶?能否作用于RNA?产生的片段末端是平末端还是黏性末端?
A:是一些随机内切酶,作用于dsDNA,产生的末端是黏性末端。
Q:产品使用时能否用单酶搭配机械法流程建库试剂盒,如 12907+12199?
A:可以。实际使用时我们建议购买完整试剂盒(Cat#12204),该试剂盒经过流程的优化可获得优异的建库表现。如果想要购买 12907 搭配其他品牌建库试剂盒,建议片段化之后先进行纯化再接其他品牌建库试剂盒。
Q:酶切模块可否适用 MGI 平台?
A:片段化酶切模块 12907可通用于各类平台
Q:gDNA 片段化参考说明书酶切条件酶切 20 min,竟然切不动?
A:一般优先考虑 DNA 的质量问题,比如 Input DNA 中引入高浓度金属离子螯合剂或其他盐离子,可能会影响酶切效果,建议将DNA 稀释在 ddH2O 或不含EDTA 的 10 mM Tris Buffer (pH 7.5-8.0)中再进行片段化。其次,如果样本是反转录得到的全长cDNA,则需考虑样本纯度问题。另外,对于环状DNA 的酶切,需要另行摸索酶切时间体系。特殊样本可考虑磁珠纯化之后进行酶切或适当延长酶切时间。
Q:酶切时间也不长,竟然过度酶切了?
A:以插入片段 300 bp 为例,白细胞 gDNA,30 度酶切 10min,出现如下图过度酶切现象。建议参考酶切条件需要考虑不同样本gDNA 大小,如白细胞gDNA 较小,应适当缩短酶切时间,否则易出现过度酶切现象。
Q:最低可以切到多小片段?
A:有小片段保护机制,最低可到150bp左右。
[1] Zhang S, Pei Z, Lei C, et al. Detection of cryptic balanced chromosomal rearrangements using high-resolution optical genome mapping [published online ahead of print, 2022 Jun 16]. J Med Genet. 2022;jmedgenet-2022-108553. doi:10.1136/jmedgenet-2022-108553(IF:6.318)
[2] Ren J, Zhang R, Pan C, et al. Prevalence and genotype-phenotype correlations of GBA-related Parkinson disease in a large Chinese cohort. Eur J Neurol. 2022;29(4):1017-1024. doi:10.1111/ene.15230(IF:6.089)
